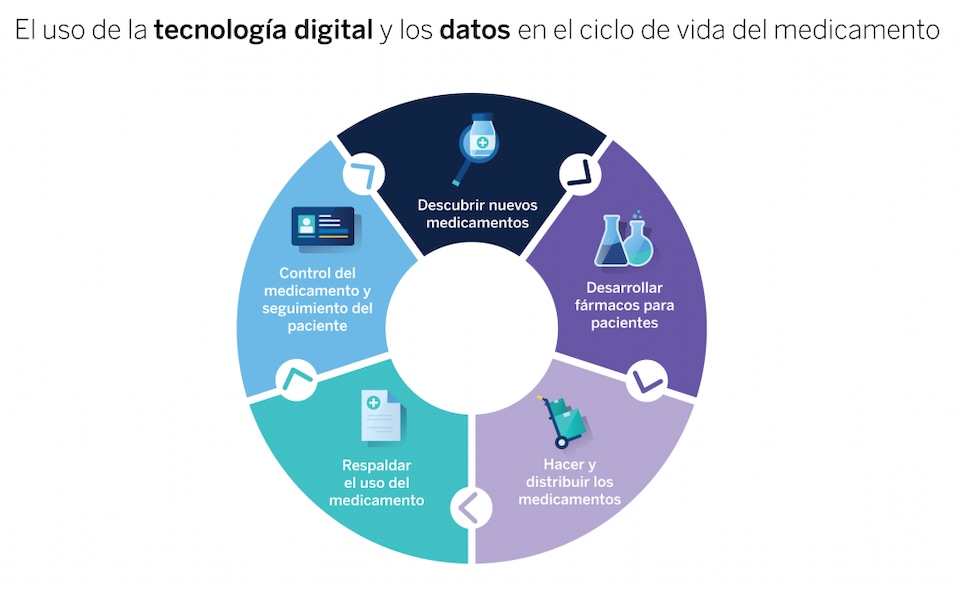
Estudiar nuevos fármacos y sus propiedades es más asequible con superordenadores e inteligencia artificial. Y en el futuro nos espera la computación cuántica. Según los expertos, la IA ha democratizado el desarrollo de medicamentos y ayuda a comprender la química y a cuestionar algunos marcos de trabajo.
En 2021 se confirmó el primer fármaco creado con inteligencia artificial, uno destinado a pacientes con la enfermedad rara de Huntington. Crear nuevos medicamentos, o nuevas funciones para los que ya existen, no es sencillo. ¿Cómo ayuda la supercomputación, el machine learning e inteligencia artificial, o la computación cuántica a descubrir nuevos medicamentos?
Se estima que existen unas 1060 combinaciones farmacológicas con los compuestos que se conocen, y probarlos todos resulta inviable cada vez que se estudia una enfermedad o dolencia.
“Las técnicas in silico (simulaciones en el ordenador, silico viene de silicio, componente básico de la computación clásica) permiten un prefiltro de sustancias conocidas”, explica Paulino Gómez-Puertas, coordinador del Grupo de Modelado Molecular del Centro de Biología Molecular Severo Ochoa (centro mixto CSIC-UAM) de Madrid, al señalar la supercomputación. “En lugar de los millones de compuestos iniciales, la simulación computacional en 3D funciona como un embudo, seleccionando algunas decenas de compuestos para las pruebas in vitro (tubo de ensayo) o in vivo (animales, humanos incluidos)”.
Por otro lado, “la inteligencia artificial y las técnicas de machine learning como deep learning se están utilizando en todas las etapas del desarrollo de fármacos”, comenta Nuria E. Campillo, científica investigadora del CSIC, divulgadora y empresaria, “que es un proceso muy largo, costoso y complejo donde, además, el ratio de fracaso es muy amplio”. Es una tecnología que ayuda a abaratar costes y democratizar el acceso a pequeñas y medianas empresas (pymes) y startups.
¿Qué aporta estos nuevos enfoques? “La principal característica del machine learning es que el sistema es capaz de aprender de forma socrática, o sea, a partir de ejemplos; y no por instrucciones”, sostiene Alejandro Pazos Sierra, doctor en medicina por la Universidad Complutense de Madrid (UCM) y doctor en ingeniería informática por la Universidad Politécnica de Madrid. Este experto señala dos características de interés: aportan soluciones a problemas complejos y tienen la capacidad de aprender y adaptarse.
El poder de la IA para pequeñas escalas
La inteligencia artificial, señala Nuria Campillo, permite diseñar de cero nuevas moléculas y esbozar sus propiedades. “El espacio químico de nuevas moléculas [las posibles combinaciones] es enorme y con herramientas clásicas lo que hacíamos era modificar moléculas existentes”. Estaban atrapados en clústeres muy compactos. Pero ahora se abre todo el espectro.
Con limitaciones, claro. La IA, nos dice Paulino Gómez-Puertas, “busca qué nuevos fármacos encajarían bien en el hueco (o centro activo) de cierta enzima”, por lo que, en lugar de partir de enormes bases de datos de compuestos ya existentes, diseñan fármacos que no existen en la naturaleza y a veces se da el problema técnico de que esa solución teórica es imposible o muy cara de sintetizar. “Y te quedas con la duda de si habría funcionado realmente o si se trata de un falso positivo de la técnica, porque no lo puedes fabricar ni, por tanto, probar”.
Otro problema asociado a los sistemas IA es su mecanismo de caja negra. Como indica Alejandro Pazos Sierra, a menudo “son incapaces de explicar el por qué llegan al resultado que obtienen”. Esto, en algunos campos como el diagnóstico médico, es crítico. El machine learning, continúa, se puede usar “para identificar moléculas candidatas a fármacos en función de la forma molecular y estructural de las proteínas diana”.
“Las enzimas [que generan o complican cierta enfermedad, como las que confieren resistencia a los antibióticos en las bacterias o facilitan la multiplicación de los virus], desde el punto de vista del volumen en tres dimensiones, son como una esfera con un hueco. Una boca llamada centro activo”, amplía Gómez-Puertas, y el enfoque es buscar compuestos químicos que ocupen este espacio. Que anulen, por tanto, la capacidad de la enzima de degradar los antibióticos en el caso de las bacterias o de amplificar la infección en el caso de los virus.
Inteligencia artificial que nos ayuda a entender la química
En 2023, el Premio Fundación BBVA Fronteras del Conocimiento en Biomedicina fue para las “contribuciones al uso de la inteligencia artificial (IA) para la predicción exacta de la estructura tridimensional de las proteínas” logrado por los proyectos AlphaFold (IA y ML para plegado de proteínas) o Rosetta@home (proyecto de computación distribuida).
Que la inteligencia artificial y el machine learning nos ayuden a comprender la química, e incluso a cuestionar algunos de los marcos de trabajo y limitadas categorías de ‘los humanos’ (por ejemplo, ¿está vivo un virus?), va a ser particularmente útil de cara a abordar retos como la aparición de superbacterias o el dar con reposicionamiento de medicamentos.
El reposicionamiento de medicamentos es fácil de comprender, se trata de encontrar efectos secundarios positivos de fármacos ya comercializados, lo que supone un ahorro en investigación, testeo y aprobación. La capacidad de las superbacterias es menos intuitiva. Paulino Gómez-Puertas lo explica así: “La resistencia a antibióticos suele ir dentro de un segmento de ADN llamado plásmido, que hay dentro de las bacterias. Las bacterias pueden físicamente transmitir el plásmido entre especies diferentes”. En hospitales, esto supone un reto.

Su futuro, nuestra mejor inversión
Predecir propiedades
En 2018, la inteligencia artificial Atom2Vec fue capaz de recrear en dos horas la tabla periódica de los elementos partiendo de una gran base de datos de moléculas. A los humanos nos llevó un siglo entender cómo ordenar esa información. Según aquel comunicado de la Universidad de Standford, la IA quizá nos ayude a “encontrar nuevas leyes de la naturaleza”.
De momento, hemos alcanzado un hecho fascinante: la capacidad predictiva de propiedades de moléculas que no hemos ensayado, gracias a que la IA aprende con una cantidad ingente de datos. En farmacología, la predictibilidad es clave, y “saber de antemano si una molécula va a ser tóxica o se va a absorber bien es muy útil”, puntualiza Nuria Campillo, quien señala la enorme reducción de costes asociada. “Una vez iniciada la investigación de una molécula, cambiarla es costoso”.
En la actualidad, Nuria Campillo y su empresa AItenea Biotech están trabajando en el diseño y optimización de moléculas y sus propiedades haciendo uso de pequeños conjuntos de datos, gracias a la aparición de algoritmos que permiten entrenar con muy pocos datos (de forma análoga a como un niño aprende que un gato es un gato: le vale con uno o dos ejemplos).
La próxima iteración de la búsqueda de medicamentos la aporta la computación cuántica. A medida que la curva de experiencia abarata el coste de nuevos métodos gracias a su masificación, estos se hacen aún más usados. Son muy visuales los siguientes ejemplos:
- Fotovoltaica. En 1975, el coste de generar 1 vatio era de más de 115 dólares estadounidenses, mientras que en 2020 rondaba los 0,27 USD.
- Análisis del genoma. En el año 2000, secuenciar el genoma costaba 1.000 millones de dólares, pero en 2015 era posible hacerlo con 1.000 dólares.
- Almacenamiento digital. En 1980, almacenar 1 GB costaba más de medio millón de dólares; y en 2020 había caído por debajo de 0,02 USD.
“La IA ha democratizado el desarrollo de fármacos y ha permitido que empresas pequeñas accedan al desarrollo de fármacos”, concluye Campillo. Cuando los algoritmos de ordenadores cuánticos estén desarrollados y exista un mercado estable de computación cuántica, no cabe duda de que estas herramientas se popularizarán entre quienes investigan.
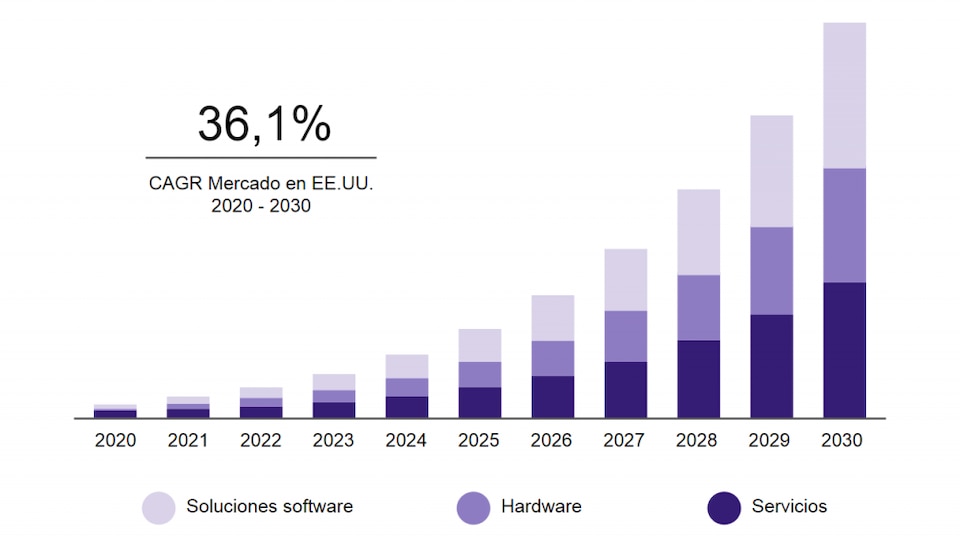
Inteligencia artificial estadounidense en el mercado de la salud (2020-2030)